Toptailieu.vn xin giới thiệu 30 bài tập trắc nghiệm Luyện tập chương 1 (có đáp án) chọn lọc, hay nhất giúp học sinh lớp 9 ôn luyện kiến thức để đạt kết quả cao trong các bài thi môn Hóa.
Mời các bạn đón xem:
Luyện tập chương 1
Câu 1: Công thức hoá học của sắt(II) oxit là
A. Fe2O3
B. Fe3O4
C. Fe3O2
D. FeO
Lời giải:
Công thức hoá học của sắt (II) oxit là FeO.
Đáp án cần chọn là:D
Câu 2: Dãy chất nào sau đây là oxit lưỡng tính?
A. Al2O3, ZnO, Cr2O3
B. Al2O3, MgO, PbO
C. CaO, ZnO, Na2O
D. PbO2, Al2O3, K2O
Lời giải:
Oxit lưỡng tính là oxit vừa tác dụng dung dịch axit, vừa tác dụng với dung dịch bazơ.
Dãy chất là oxit lưỡng tính là Al2O3, ZnO, Cr2O3
Đáp án cần chọn là:A
Câu 3: Hòa tan hoàn toàn 8,1 gam một oxit kim loại hóa trị II cần vừa đủ 0,2 mol axit HCl. Oxit đó là
A. MgO
B. FeO
C. CuO
D. ZnO
Lời giải:
Gọi công thức của oxit là MO
Phương trình phản ứng:
Số mol của MO là:
nMO = 0,1 mol
MMO = = 81 g/mol
Suy ra MM + MO = 81
MM = 81 – MO
MM = 81 – 16 = 65 g/mol
Suy ra M là Zn
Vậy công thức oxit là ZnO
Đáp án cần chọn là:D
Câu 4: Vôi sống có công thức hóa học là
A. CaO
B. Ca
C. Ca(OH)2
D. CaCO3
Lời giải:
Vôi sống có công thức hóa học là CaO.
Đáp án cần chọn là:A
Câu 5: Cho 11,2 gam kim loại sắt tác dụng vừa đủ với dung dịch axit sunfuric loãng. Thể tích khí hiđro thu được ở đktc là
A. 2,24 lít
B. 4,48 lít
C. 5,60 lít
D. 6,05 lít
Lời giải:
Số mol Fe là:
nFe = 0,2 mol
Phương trình phản ứng:
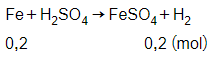
Theo phương trình phản ứng ta có:
= 0,2 mol
Thể tích khí hiđro thu được ở đktc là:
= 0,2.22,4 = 4,48 lít.
Đáp án cần chọn là:B
Câu 6: Phương trình hóa học nào sau đây đúng?
A. K2O + H2O → KOH
B. KOH + CO2 → K2CO3 + H2O
C. K2CO3 + H2SO4 → K2SO4 + CO2 + H2O
D. K2SO4 + BaCl2 → BaSO4 + KCl
Lời giải:
Phương trình hóa học đúng là:
K2CO3 + H2SO4 → K2SO4 + CO2 + H2O
Các phản ứng A, B, D đều chưa cân bằng.
Đáp án cần chọn là:C
Câu 7: Hòa tan hết CaCO3 cần vừa đủ 100 ml dung dịch HCl 2M, sau phản ứng thu được khối lượng muối là
A. 8,6 gam
B. 9,8 gam
C. 10,2 gam
D. 11,1 gam
Lời giải:
Số mol HCl là:
nHCl = 0,2 mol
Phương trình phản ứng:
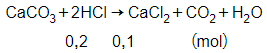
Theo phương trình phản ứng ta có:
= 0,1 mol
Khối lượng CaCl2 là:
= 0,1.111 = 11,1 gam.
Đáp án cần chọn là:D
Câu 8: Dung dịch Ca(OH)2 không có tính chất hoá học nào sau đây?
A. Làm đổi màu quỳ tím
B. Tác dụng với oxit axit tạo thành muối và nước
C. Bị nhiệt phân hủy khi đun nóng tạo thành oxit bazơ và nước
D. Tác dụng với axit tạo thành muối và nước
Lời giải:
Dung dịch Ca(OH)2 không có tính chất: bị nhiệt phân hủy khi đun nóng tạo thành oxit bazơ và nước
Vì dung dịch Ca(OH)2 là bazơ tan.
Đáp án cần chọn là:C
Câu 9: Để có được dung dịch KCl 40%, thì khối lượng KCl cần lấy hoà tan vào 150 gam nước là
A. 100 gam
B. 150 gam
C. 200 gam
D. 90 gam
Lời giải:
Ta có:
Suy ra 0,6mKCl = 60
Vậy mKCl = 100 gam
Đáp án cần chọn là:A
Câu 10: Diêm tiêu kali được dùng để chế tạo thuốc nổ đen, đồng thời được dùng làm phân bón. Công thức hóa học của diêm tiêu kali là
A. KNO3
B. KCl
C. K2CO3
D. K2SO4
Lời giải:
Diêm tiêu kali được dùng để chế tạo thuốc nổ đen, đồng thời được dùng làm phân bón. Công thức hóa học của diêm tiêu kali là KNO3.
Đáp án cần chọn là:A
Câu 11: Phương trình hóa học nào sau đây đúng?
A. CaCO3 + HCl → CaCl2 + CO + H2O
B. CaCO3 + HCl → CaO + Cl2 + H2O
C. CaCO3 + HCl → Ca(OH)2 + CO2 + HCl
D. CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Lời giải:
Phương trình hóa học viết đúng là:
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Đáp án cần chọn là:D
Câu 12: Thả một mảnh nhôm vào ống nghiệm chứa dung dịch CuSO4. Xảy ra hiện tượng
A. Có chất khí bay ra, dung dịch không đổi màu
B. Không có dấu hiệu phản ứng
C. Có chất rắn màu trắng bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần
D. Có chất rắn màu đỏ bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần
Lời giải:
Nhôm đứng trước đồng trong dãy điện hóa do đó sẽ đẩy đồng ra khỏi muối
Phương trình phản ứng:
3CuSO4 + 2Al → 3Cu + Al2(SO4)3
Hiện tượng: Có chất rắn màu đỏ bám ngoài lá nhôm, màu xanh của dung dịch CuSO4 nhạt dần.
Đáp án cần chọn là:D
Câu 13: Dãy bazơ nào sau đây gồm các bazơ không tan?
A. NaOH, KOH, Cu(OH)2
B. Ca(OH)2, Mg(OH)2, Ba(OH)2
C. Mg(OH)2, Fe(OH)3, Al(OH)3
D. Al(OH)3, KOH, Zn(OH)2
Lời giải:
Dãy gồm các bazơ không tan là:
Mg(OH)2, Fe(OH)3, Al(OH)3
Đáp án cần chọn là:C
Câu 14: Cho 0,3 mol CuCl2 phản ứng với một dung dịch có hòa tan 32 gam NaOH, thu được m gam kết tủa. Giá trị của m là
A. 26,7 gam
B. 27,9 gam
C. 28,6 gam
D. 29,4 gam
Lời giải:
Số mol NaOH là:
nNaOH = 0,8 mol
Phương trình phản ứng:
CuCl2 + 2NaOH → Cu(OH)2 + 2NaCl
Xét
CuCl2 phản ứng hết, NaOH dư.
Theo phương trình phản ứng ta có:
= 0,3 mol
Vậy khối lượng Cu(OH)2 là:
= 0,3.98 = 29,4 gam.
Đáp án cần chọn là:D
Câu 15: Để một mẫu natri hidroxit trên tấm kính trong không khí, sau vài ngày thấy có chất rắn màu trắng phủ ngoài. Nếu nhỏ vài giọt dung dịch HCl vào chất rắn trắng thấy có chất khí thoát ra, khí này làm đục nước vôi trong. Chất rắng màu trắng là sản phẩm phản ứng natri hidroxit với
A. Cacbon đioxit trong không khí
B. Oxi trong không khí
C. Hơi nước trong không khí
D. Cacbon đioxit và oxi trong không khí
Lời giải:
Phương trình phản ứng:
2NaOH + CO2 → Na2CO3 + H2O
Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
Đáp án cần chọn là:A
Câu 16: Có 3 lọ mất nhãn đựng riêng biệt 3 dung dịch của 3 chất: HCl, Na2SO4, NaOH . Chỉ dùng một hóa chất nào sau đây để phân biệt chúng ?
A. Dung dịch BaCl2
B. Quỳ tím
C. Dung dịch Ba(OH)2
D. Zn
Lời giải:
Sử dụng quỳ tím:
+ Quỳ tím chuyển sang màu đỏ → HCl
+ Quỳ tím chuyển sang màu xanh → NaOH
+ Quỳ tím không chuyển màu → Na2SO4.
Đáp án cần chọn là:B
Câu 17: Khi cho từ từ dung dịch NaOH cho đến dư vào ống nghiệm đựng dung dịch hỗn hợp gồm HCl và một ít phenolphtalein. Hiện tượng quan sát được trong ống nghiệm là:
A. Màu đỏ mất dần.
B. Không có sự thay đổi màu
C. Màu đỏ từ từ xuất hiện.
D. Màu xanh từ từ xuất hiện.
Lời giải:
Trong dung dịch sau phản ứng có NaOH dư làm cho phenolphtalein chuyển sang màu đỏ.
Đáp án cần chọn là:C
Câu 18: Cho 0,1mol kim loại kẽm vào dung dịch HCl dư. Khối lượng muối thu được là:
A. 13,6 g
B. 1,36 g
C. 20,4 g
D. 27,2 g
Lời giải:
→ mmuối = 0,1.(65 + 35,5.2) = 13,6 gam.
Đáp án cần chọn là:A
Câu 19: Cho 0,2 mol Canxi oxit tác dụng với 500ml dung dịch HCl 1M. Khối lượng muối thu được là:
A. 2,22 g
B. 22,2 g
C. 23,2 g
D. 22,3 g
Lời giải:
nHCl = 0,5.1 = 0,5 mol
Có 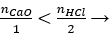
mmuối = 0,2. (40 + 71) = 22,2 gam.
Đáp án cần chọn là:B
Câu 20: Dung dịch axit clohiđric tác dụng với sắt tạo thành:
A. Sắt (II) clorua và khí hiđrô.
B. Sắt (III) clorua và khí hiđrô.
C. Sắt (II) Sunfua và khí hiđrô.
D. Sắt (II) clorua và nước.
Lời giải:
Fe + 2HCl → FeCl2 + H2
Đáp án cần chọn là:A
Câu 21: Dung dịch muối tác dụng với dung dịch axit clohiđric là:
A. Zn(NO3)2
B. NaNO3.
C. AgNO3.
D. Cu(NO3)2.
Lời giải:
AgNO3 + HCl → AgCl ↓ + HNO3
Đáp án cần chọn là:C
Câu 22: Axit sunfuric đặc nóng tác dụng với đồng kim loại sinh ra khí:
A. CO2.
B. SO2.
C. SO3.
D. H2S.
Lời giải:
Đáp án cần chọn là:B
Câu 23: Dãy các kim loại đều tác dụng với dung dịch axit clohiđric:
A. Al, Cu, Zn, Fe.
B. Al, Fe, Mg, Ag.
C. Al, Fe, Mg, Cu.
D. Al, Fe, Mg, Zn.
Lời giải:
Cu và Ag không tác dụng với axit HCl.
Đáp án cần chọn là:D
Câu 24: Thuốc thử để nhận biết dung dịch Ca(OH)2 là
A. K2CO3
B. KCl
C. KOH
D. KNO3
Lời giải:
Ca(OH)2 + K2CO3 → CaCO3 ↓ + 2KOH
Đáp án cần chọn là:A
Câu 25: Hòa tan 3,1 gam Na2O vào nước được 2 lít dung dịch. Nồng độ mol của dung dịch thu được là:
A. 0,05 M
B. 0,1 M
C. 0,3M
D. 0,4M
Lời giải:
Số mol Na2O = 3,1 : 62 = 0,05 mol
Đáp án cần chọn là:A
Câu 26: Có 3 lọ mất nhãn đựng riêng biệt 3 dung dịch của 3 chất: HCl, Na2SO4, NaOH . Chỉ dùng một hóa chất nào sau đây để phân biệt chúng ?
A. Dung dịch BaCl2
B. Quỳ tím
C. Dung dịch Ba(OH)2
D. Zn
Lời giải:
Sử dụng quỳ tím:
+ Quỳ tím chuyển sang màu đỏ → HCl
+ Quỳ tím chuyển sang màu xanh → NaOH
+ Quỳ tím không chuyển màu → Na2SO4.
Đáp án cần chọn là:B
Câu 27: Khi cho từ từ dung dịch NaOH cho đến dư vào ống nghiệm đựng dung dịch hỗn hợp gồm HCl và một ít phenolphtalein. Hiện tượng quan sát được trong ống nghiệm là:
A. Màu đỏ mất dần.
B. Không có sự thay đổi màu
C. Màu đỏ từ từ xuất hiện.
D. Màu xanh từ từ xuất hiện.
Lời giải:
Trong dung dịch sau phản ứng có NaOH dư làm cho phenolphtalein chuyển sang màu đỏ.
Đáp án cần chọn là:C
Câu 28: Cho 0,1mol kim loại kẽm vào dung dịch HCl dư. Khối lượng muối thu được là:
A. 13,6 g
B. 1,36 g
C. 20,4 g
D. 27,2 g
Lời giải:
→ mmuối = 0,1.(65 + 35,5.2) = 13,6 gam.
Đáp án cần chọn là:A
Câu 29: Cho 0,2 mol Canxi oxit tác dụng với 500ml dung dịch HCl 1M. Khối lượng muối thu được là:
A. 2,22 g
B. 22,2 g
C. 23,2 g
D. 22,3 g
Lời giải:
nHCl = 0,5.1 = 0,5 mol
Có 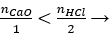
mmuối = 0,2. (40 + 71) = 22,2 gam.
Đáp án cần chọn là:B
Câu 30: Dung dịch axit clohiđric tác dụng với sắt tạo thành:
A. Sắt (II) clorua và khí hiđrô.
B. Sắt (III) clorua và khí hiđrô.
C. Sắt (II) Sunfua và khí hiđrô.
D. Sắt (II) clorua và nước.
Lời giải:
Fe + 2HCl → FeCl2 + H2
Đáp án cần chọn là:A
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.