Toptailieu.vn xin giới thiệu 15 câu trắc nghiệm Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố trong một nhóm Kết nối tri thức (có đáp án 2023) CHỌN LỌC, hay nhất giúp học sinh lớp 10 ôn luyện kiến thức để đạt kết quả cao trong các bài thi môn Hóa học.
Mời các bạn đón xem:
15 câu trắc nghiệm Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố trong một nhóm Kết nối tri thức (có đáp án 2023) CHỌN LỌC
Lý thuyết
I. Cấu hình electron nguyên tử của các nguyên tố nhóm A
Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố nhóm A
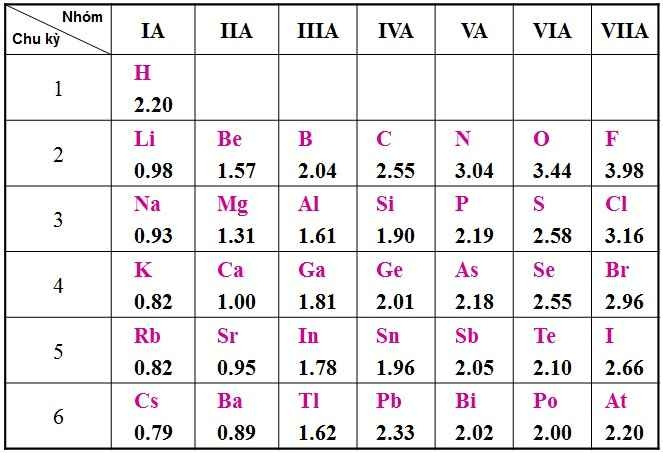
- Nhóm A gồm các nguyên tố s và p. Nguyên tử của các nguyên tố cùng một nhóm A có số electron ngoài cùng (electron hóa trị) bằng nhau (trừ He trong nhóm VIIIA)
- Sự giống nhau về số electron hóa trị dẫn đến sự tương tự nhau về tính chất hóa học của các nguyên tố trong cùng nhóm A
- Sau mỗi chu kì, cấu hình electron ngoài cùng của nguyên tử các nguyên tố nhóm A được lặp đi lặp lại một cách tuần hoàn. Sự biến đổi tuần hoàn cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố khi điện tích hạt nhân tăng dần là nguyên nhân của sự biến đổi tuần hoàn về tính chất của các nguyên tố
II. Bán kính nguyên tử
- Một cách gần đúng, bán kính nguyên tử được xác định bằng nửa khoảng cách trung bình giữa 2 hạt nhân nguyên tử gần nhau nhất trong chất rắn đơn chất hoặc trong phân tử hai nguyên tử giống nhau
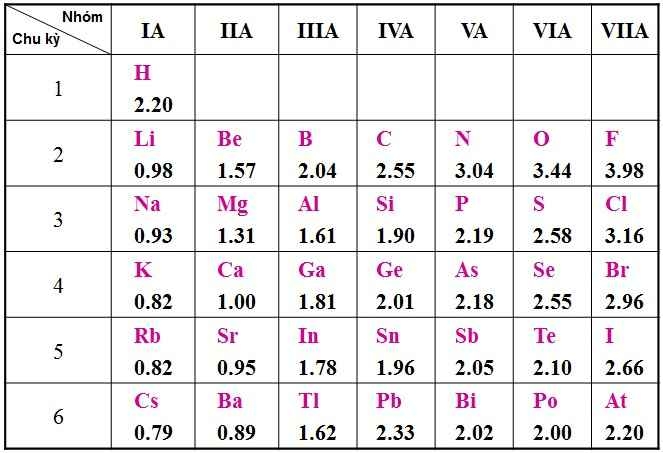
Sự giảm bán kính nguyên tử của các nguyên tố trong chu kì 3
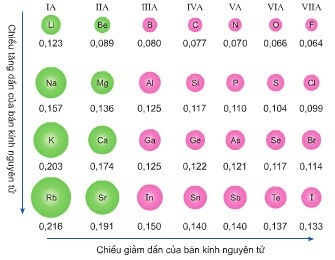
Giá trị bán kính nguyên tử
- Bán kính nguyên tử phụ thuộc vào lực hút giữa hạt nhân với các electron lớp ngoài cùng. Bán kính giảm là do lực hút tăng và ngược lại, bán kính tăng là do lực hút giảm
- Xu hướng biến đổi bán kính nguyên tử
+ Trong 1 chu kì, bán kính nguyên tử giảm dần theo chiều tăng dần của điện tích hạt nhân
+ Trong 1 nhóm A, bán kính nguyên tử tăng theo chiều tăng dần điện tích hạt nhân
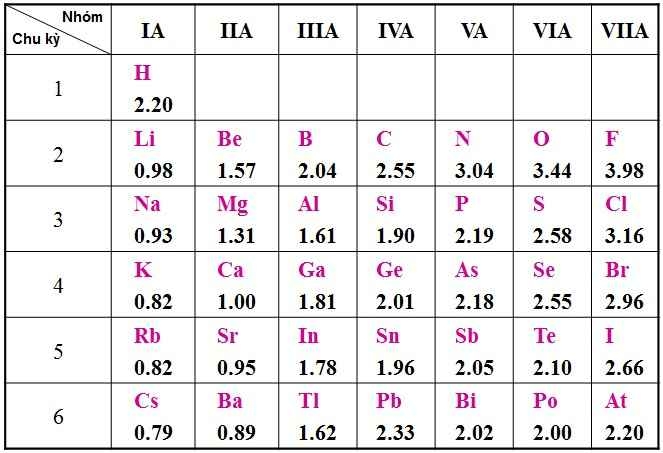
Sự biến đổi năng lượng ion hóa thứ nhất của các nguyên tố chu kì 2 và 3
- Năng lượng ion hóa thứ nhất của nguyên tử là năng lượng tối thiểu cần thiết để tách electron thứ nhất ra khỏi nguyên tử ở thể khí, trạng thái cơ bản:
- Năng lượng ion hóa thứ nhất kí hiệu là I1, đơn vị là kJ/mol
Ví dụ: Để tách một mol electron ra khỏi một mol nguyên tử hydrogen theo quá trình H(g) → H+(g) + e phải tiêu tốn một năng lượng là 1312 kJ, do đó I1 = 1312 kJ/mol
+ Trong một chu kì, năng lượng ion hóa thứ nhất có xu hướng tăng theo chiều tăng dần của điện tích hạt nhân
+ Trong một nhóm A, năng lượng ion hóa thứ nhất có xu hướng giảm theo chiều tăng dần của điện tích hạt nhân
III. Độ âm điện
- Độ âm điện của nguyên tử là đại lượng đặc trưng cho khả năng hút electron của nguyên tử một nguyên tố hóa học khi tạc thành liên kết hóa học
- Khi tham gia liên kết hóa học, nguyên tử có độ âm điện nhỏ dễ nhường electron, nguyên tử có độ âm điện lớn dễ nhận electron
- Xu hướng biến đổi độ âm điện theo chiều tăng dần của điện tích hạt nhân
+ Độ âm điện tăng từ trái qua phải trong một chu kì
- Trong một chu kì, khi số electron lớp ngoài cùng tăng, điện tích hạt nhân tăng thì lực hút giữa hạt nhân với các electron ngoài cùng tăng nên độ âm điện tăng
+ Độ âm điện giảm từ trên xuống trong một nhóm A
- Trong một nhóm A, khi số lớp electron tăng, lực hút giữa hạt nhân với các electron lớp ngoài cùng giảm nên độ âm điện giảm
IV. Tính kim loại và tính phi kim
1. Khái niệm
- Tính kim loại là tính chất của một nguyên tố mà nguyên tử của nó dễ nhường electron để trở thành ion dương. Nguyên tử của nguyên tố nào càng dễ nhường electron để trở thành ion dương, tính kim loại của nguyên tố đó càng mạnh.
- Tính phi kim là tính chất của một nguyên tố mà nguyên tử của nó dễ nhường electron để trở thành ion âm. Nguyên tử của nguyên tố nào càng dễ nhận electron để trở thành ion âm, tính phi kim của nguyên tố đó càng mạnh.
2. Sự biến đổi tính kim loại, tính phi kim
Ví dụ: So sánh tính kim loại của sodium và magnesium
- Chuẩn bị: Kim loại Na, Mg, dung dịch phenolphtalein, nước, cốc thủy tinh
- Tiến hành:
+ Lấy 2 cốc thủy tinh, mỗi cốc chứa khoảng 200 ml nước, nhỏ tiếp vài giọt dung dịch
+ Cho 1 mẫu nhỏ Na vào cốc (1), một dây Mg vào cốc (2)
Lưu ý: hầu hết kim loại kiềm phản ứng với nước mãnh liệt, chỉ sử dụng các kim loại kiềm với lượng nhỏ, cần làm sạch bề mặt dây Mg trước khi cho vào cốc (2)
Phương trình phản ứng:
2Na + 2H2O → 2NaOH + H2
Mg + 2H2O → Mg(OH)2 + H2
Quan sát thí nghiệm có thể thấy kim loại Na tác dụng mãnh liệt với nước còn Mg tác dụng chậm hơn, điều này chứng tỏ kim loại Na dễ nhường electron để trở thành ion dương hơn so với Mg nên Na có tính kim loại mạnh hơn Mg
- Xu hướng biến đổi tính kim loại và phi kim
+ Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính kim loại giảm dần và tính phi kim tăng dần. Do bán kính nguyên tử giảm, lực hút giữa hạt nhân với các electron lớp ngoài cùng tăng, dẫn đến khả năng nhường electron giảm nên tính kim loại giảm, khả năng nhận electron tăng nên tính phi kim tăng
+ Trong một nhóm A, theo chiều tăng dần của điện tích hạt nhân, tính kim loại tăng dần và tính phi kim giảm dần. Tuy điện tích hạt nhân tăng dần, nhưng bán kính nguyên tử tăng nhanh hơn, lực hút giữa hạt nhân với các electron lớp ngoài cùng giảm, dẫn đến khả năng nhường electron tăng nên tính kim loại tăng, khả năng nhận electron giảm nên tính phi kim giảm.
Ví dụ:
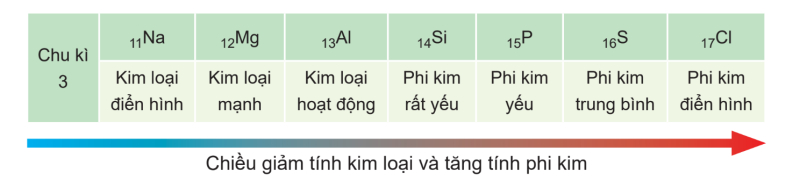
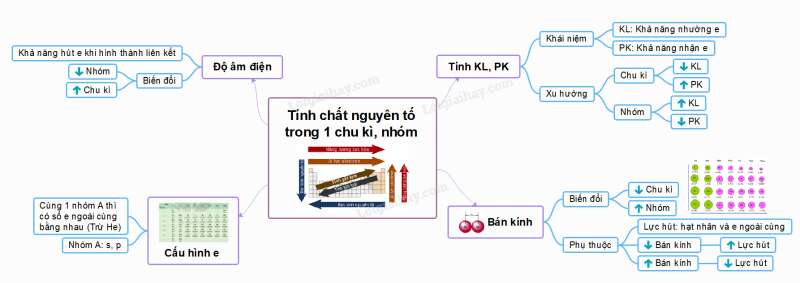
Bài tập
Câu 1. Nhóm A gồm các nguyên tố nào?
A. Nguyên tố s;
B. Nguyên tố p;
C. Nguyên tố s và p;
D. Nguyên tố d.
Đáp án: C
Nhóm A gồm các nguyên tố s và p.
Câu 2. Yếu tố nào ảnh hưởng nhiều nhất đến tính chất hóa học của nguyên tố nhóm A?
A. Cấu hình electron nguyên tử;
B. Số khối;
C. Khối lượng nguyên tử.
D. Số neutron.
Đáp án: A
Nguyên tử của các nguyên tố cùng một nhóm A có số electron lớp ngoài cùng bằng nhau (trừ He trong nhóm VIIIA). Sự giống nhau về số electron hóa trị dẫn đến sự tương tự nhau về tính chất hóa học của các nguyên tố trong cùng nhóm A.
Câu 3. Khi xếp theo chiều tăng dần của điện tích hạt nhân, đại lượng nào sau đây không biến đổi tuần hoàn?
A. Bán kính nguyên tử;
B. Số neutron;
C. Tính kim loại, tính phi kim;
D. Độ âm điện.
Đáp án: B
Khi xếp theo chiều tăng dần của điện tích hạt nhân, số neutron không biến đổi tuần hoàn.
- Trong một chu kì:
+ Bán kính nguyên tử giảm dần, độ âm điện tăng dần.
+ Tính kim loại giảm dần và tính phi kim tăng dần
- Trong một nhóm A:
+ Bán kính nguyên tử tăng dần, độ âm điện giảm dần.
+ Tính kim loại tăng dần và tính phi kim giảm dần.
Câu 4. Dãy nguyên tố nào sau đây sắp xếp theo chiều tăng dần của bán kính nguyên tử?
A. Li, Na, K, Rb;
B. Ca, Mg, Al, P;
C. Cl, S, O, N;
D. Br, I, Ca, Al.
Đáp án: A
Li, Na, K, Rb đều thuộc nhóm IA.
Trong một nhóm A, bán kính nguyên tử tăng theo chiều tăng dần của điện tích hạt nhân.
Câu 5. Bán kính nguyên tử phụ thuộc vào yếu tố nào?
A. Cấu hình electron nguyên tử;
B. Khối lượng nguyên tử.
C. Năng lượng ion hóa;
D. Lực hút giữa hạt nhân với các electron lớp ngoài cùng.
Đáp án: D
Bán kính nguyên tử phụ thuộc vào lực hút giữa hạt nhân với các electron lớp ngoài cùng. Bán kính giảm là do lực hút tăng và ngược lại, bán kính tăng là do lực hút giảm.
Câu 6. Dãy nguyên tố nào sau đây sắp xếp theo chiều giảm dần của bán kính nguyên tử?
A. S, P, Cl, O;
B. Ca, Mg, K, Br;
C. Mg, Al, P, S;
D. Na, Mg, K, Ca.
Đáp án: C
Mg, Al, P, S đều thuộc chu kì 3.
Trong một chu kì, bán kính nguyên tử giảm theo chiều tăng dần của điện tích hạt nhân.
Câu 7. Phát biểu nào sau đây không đúng về năng lượng ion hóa thứ nhất?
A. Năng lượng ion hóa thứ nhất của nguyên tử là năng lượng tối thiểu cần thiết để tách electron thứ nhất ra khỏi nguyên tử ở thế khí;
B. Năng lượng ion hóa thứ nhất kí hiệu là I1, đơn vị là kJ.mol;
C. Trong một chu kì, năng lượng ion hóa thứ nhất có xu hướng tăng theo chiều tăng dần của điện tích hạt nhân.
D. Trong một nhóm A, năng lượng ion hóa thứ nhất có xu hướng giảm theo chiều tăng dần của điện tích hạt nhân.
Đáp án: B
Năng lượng ion hóa thứ nhất kí hiệu là I1, đơn vị là kJ/mol.
Câu 8. Đại lượng nào đặc trưng cho khả năng hút electron của nguyên tử một nguyên tố hóa học khi tạo thành liên kết hóa học?
A. Bán kính nguyên tử;
B. Cấu hình electron nguyên tử;
C. Năng lượng ion hóa;
D. Độ âm điện.
Đáp án: D
Độ âm điện của nguyên tử là đại lượng đặc trưng cho khả năng hút electron của nguyên tử một nguyên tố hóa học khi tạo thành liên kết hóa học.
Khi tham gia liên kết hóa học, nguyên tử có độ âm điện nhỏ dễ nhường electron, nguyên tử có độ âm điện lớn dễ nhận electron.
Câu 9. Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân
A. Bán kính giảm dần, tính kim loại giảm;
B. Bán kính tăng dần, tính kim loại tăng;
C. Bán kính tăng dần, tính phi kim tăng;
D. Bán kính giảm dần, tính phi kim giảm.
Đáp án: A
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, bán kính giảm dần, tính kim loại giảm và tính phi kim tăng dần.
Câu 10. Trong một nhóm A, theo chiều tăng dần của điện tích hạt nhân
A. Bán kính giảm dần, tính kim loại giảm;
B. Bán kính tăng dần, tính kim loại tăng;
C. Bán kính tăng dần, tính phi kim tăng;
D. Bán kính giảm dần, tính phi kim giảm.
Đáp án: B
Trong một nhóm A, theo chiều tăng dần của điện tích hạt nhân bán kính tăng dần, tính kim loại tăng và tính phi kim giảm dần.
Câu 11. Dãy nguyên tố nào sau đây sắp xếp theo chiều tăng dần độ âm điện?
A. Na, K, Rb, Li;
B. Li, Rb, Na, K;
C. Rb, K, Na, Li;
D. Na, Li, K, Rb.
Đáp án: C
Li, Na, K, Rb đều thuộc nhóm IA nên độ âm điện của Rb < K < Na < Li.
Câu 12. Dãy nguyên tố nào sau đây sắp xếp theo chiều tăng dần tính kim loại?
A. F, Be, N, O;
B. O, N, Be, F;
C. F, O, N, Be;
D. F, Be, O, N.
Đáp án: C
O, N, Be, F đều thuộc chu kì 2 nên tính kim loại của Be > N > O > F.
Câu 13. Nguyên tử nguyên tố nào sau đây có bán kính nhỏ nhất?
A. Li;
B. Na;
C. K;
D. Cs.
Đáp án: A
Li, Na, K, Cs đều thuộc nhóm IA nên Li có bán kính nhỏ nhất.
Câu 14. Chỉ ra nội dung sai: Tính phi kim của nguyên tố càng mạnh thì?
A. Khả năng nhận electron càng mạnh;
B. Độ âm điện càng lớn;
C. Bán kính nguyên tử càng lớn;
D. Tính kim loại càng yếu.
Đáp án: C
Trong một chu kì, theo chiều tăng dần điện tích hạt nhân, bán kính nguyên tử giảm dần, lực hút giữa hạt nhân với các electron lớp ngoài cùng tăng dẫn đến khả năng nhường electron giảm, khả năng nhận electron tăng nên tính phi kim tăng.
Câu 15. Cho các phát biểu sau:
(1) F là phi kim mạnh nhất;
(2) Li có độ âm điện nhỏ nhất;
(3) H có bán kính nguyên tử nhỏ nhất;
(4) P là phi kim hoạt động mạnh nhất.
Số phát biểu đúng là?
A. 1;
B. 2;
C. 3;
D. 4.
Đáp án: A
Chỉ có phát biểu (1) đúng.
Xem thêm các bài giải Trắc nghiệm Hóa lớp 10 Kết nối tri thức hay, chi tiết khác:
Bài 5: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
Bài 7: Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kỳ
Bài 8: Định luật tuần hoàn. Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.