Toptailieu.vn xin giới thiệu 15 câu trắc nghiệm Liên kết ion Cánh diều (có đáp án 2023) CHỌN LỌC, hay nhất giúp học sinh lớp 10 ôn luyện kiến thức để đạt kết quả cao trong các bài thi môn Hóa học.
Mời các bạn đón xem:
15 câu trắc nghiệm Liên kết ion Cánh diều (có đáp án 2023) CHỌN LỌC
Lý thuyết
I. Sự tạo thành ion
Kim loại điển hình phản ứng rất mạnh với phi kim điển hình tạo ra hợp chất ion. Khi đó, nguyên tử kim loại nhường electron để tạo thành ion mang điện tích dương (cation) còn nguyên tử phi kim nhận electron để trở thành ion mang điện tích âm (anion).
Ví dụ 1:
Cấu hình electron của nguyên tử Na (Z = 11): 1s22s22p63s1
→ Có 1 electron ở lớp ngoài cùng.
Nguyên tử Na nhường đi 1 electron ở lớp ngoài cùng để tạo thành ion dương Na+ (cation sodium).
Na → Na+ + 1e
Chú ý: Số đơn vị điện tích của ion dương (cation) bằng số electron mà nguyên tử đã nhường.
Ví dụ 2:
Cấu hình electron của nguyên tử Cl (Z = 17): 1s22s22p63s23p5.
→ Có 7 electron ở lớp ngoài cùng.
Nguyên tử Cl nhận 1 electron để tạo thành ion âm Cl- (anion chloride).
Cl + 1e → Cl-
Chú ý: Số đơn vị điện tích của ion âm (anion) bằng số electron mà nguyên tử đã nhận.
Các ion thường có cấu hình electron bền vững của nguyên tử khí hiếm gần nhất với nguyên tố tạo thành ion đó trong bảng tuần hoàn.
II. Sự tạo thành liên kết ion
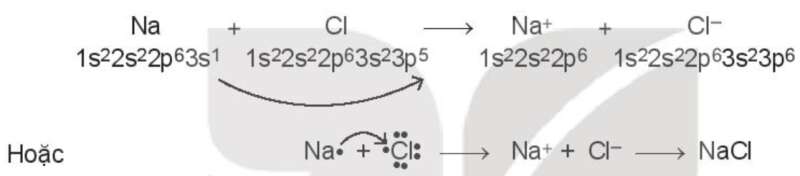
Ví dụ 1: Xét sự tạo thành liên kết hóa học trong phân tử sodium chloride (NaCl):
Khi kim loại sodium kết hợp với phi kim chlorine, tạo thành các ion Na+ và Cl-, các ion này mang điện tích trái dấu sẽ hút nhau tạo thành liên kết ion.
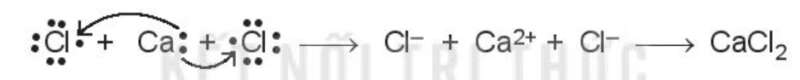
Ví dụ 2: Xét sự thành thành liên kết hóa học trong phân tử calcium chloride (CaCl2):
Khi kim loại calcium kết hợp với phi kim chlorine, tạo thành các ion Ca2+ và Cl-. Các ion này mang điện tích trái dấu sẽ hút nhau tạo thành liên kết ion.
Kết luận:
- Lực hút tĩnh điện giữa các ion mang điện trái dấu trong phân tử (hay tinh thể) tạo ra liên kết ion.
- Liên kết ion thường được hình thành giữa kim loại điển hình và phi kim điển hình. Các hợp chất tạo nên từ các ion được gọi là những hợp chất ion.
III. Tinh thể ion
1. Cấu trúc của tinh thể ion
Các ion được sắp xếp theo một trật tự xác định trong không gian theo kiểu mạng lưới, trong đó ở các nút của mạng lưới là những ion dương và ion âm được sắp xếp luân phiên, liên kết chặt chẽ với nhau do sự cân bằng giữa lực hút (các ion trái dấu hút nhau) và lực đẩy (các ion cùng dấu đẩy nhau), tạo thành mạng tinh thể ion.
Ví dụ: Tinh thể muối ăn.
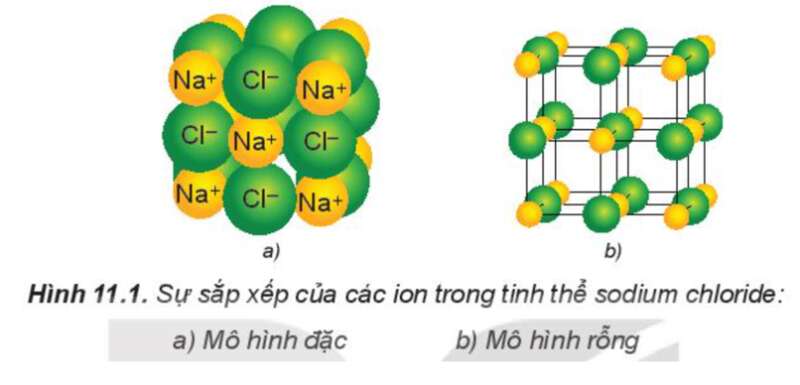
2. Độ bền và tính chất của hợp chất ion
Tron tinh thể ion, giữa các ion có lực hút tĩnh điện rất mạnh nên các hợp chất ion thường là chất rắn, khó nóng chảy, khó bay hơi ở điều kiện thường.
Các tinh thể ion khá rắn chắc, nhưng khá giòn. Đây là tính chất đặc trưng của tinh thể ion.
Ví dụ: Tinh thể muối ăn ở dạng rắn, cứng, nhưng khi tác dụng một lực mạnh thì vỡ vụn.
Các hợp chất ion có khả năng dẫn điện khi tan trong nước hay khi nóng chảy.
Bài tập
Câu 1: Liên kết ion được tạo thành giữa
A. hai nguyên tử kim loại.
B. hai nguyên tử phi kim.
C. một nguyên tử kim loại mạnh và một nguyên tử phi kim mạnh.
D. một nguyên tử kim loại yếu và một nguyên tử phi kim yếu.
Đáp án: C
Câu 2: Trong tinh thể NaCl, nguyên tố Na và Cl ở dạng ion và có sô electron lần lượt là
A. 10 và 18 B. 12 và 16 C. 10 và 10 D. 11 và 17
Đáp án: A
Câu 3: Phân tử nào sau đây có liên kết phân cực nhất?
A. F2O B. Cl2O C. ClF D. O2
Đáp án: C
Câu 4: Liên kết trong phân tử chất nào sau đây mang nhiều tính chất của liên kết ion nhất?
A. LiCl B. NaCl C. KCl D. CsCl
Đáp án: D
Câu 5: Các chất trong dãy nào sau đây đều có liên kết ion?
A. KBr, CS2, MgS
B. KBr, MgO, K2O
C. H2O, K2O, CO2
D. CH4, HBr, CO2
Đáp án: B
Câu 6: Hợp chất trong phân tử có liên kết ion là
A. HCl B. NH3 C. H2O D. NH4Cl
Đáp án: D
Câu 7: Nguyên tử của nguyên tố X có cấu hình electron 1s22s22p63s23p64s1, nguyên tử của nguyên tố Y có cấu hình electron 1s22s22p5. Liên kết hóa học giữa nguyên tử X và nguyên tử Y thuộc loại liên kết
A. kim loại. B. cộng hóa trị. C. ion. D. cho – nhận.
Đáp án: C
X là K (kim loại mạnh), Y là phi kim (phi kim yếu)
Liên kết hóa học giữa X và Y là liên kết ion
Câu 8: X, Y là những nguyên tố có điện tích hạt nhân lần lượt là 9, 19.
Cấu hình electron lớp ngoài cùng của nguyên tử X, Y và liên kết trong hợp chất tạo thành từ X và Y là
A. 2s22p5, 4s1 và liên kết cộng hóa trị.
B. 2s22p3, 3s23p1 và liên kết cộng hóa trị.
C. 3s23p1, 4s1 và liên kết ion.
D. 2s22p1, 4s1 và liên kết ion.
Đáp án: D
Câu 9: Nhóm hợp chất nào sau đây đều là hợp chất ion ?
A. H2S, Na2O. B. CH4, CO2.
C. CaO, NaCl. D. SO2, KCl.
Đáp án: C
Câu 10: Hầu hết các hợp chất ion
A. có nhiệt độ nóng chảy và nhiệt độ sôi cao.
B. dễ hòa tan trong các dung môi hữu cơ.
C. ở trạng thái nóng chảy không dẫn điện.
D. tan trong nước thành dung dịch không điện li.
Đáp án: A
Câu 11: Bản chất của liên kết ion là lực hút tĩnh điện giữa
A. 2 ion.
B. 2 ion mang điện trái dấu.
C. các hạt mang điện trái dấu.
D. hạt nhân và các electron hóa trị.
Đáp án: B
Câu 12: Điện hóa trị của Mg và Cl trong MgCl2 theo thứ tự là :
A. 2 và 1.
B. 2+ và 1–.
C. +2 và –1.
D. 2+ và 2–
Đáp án: B
Câu 13: Hợp chất trong phân tử có liên kết ion là :
A. NH4Cl.
B. HCl.
C. NH3.
D. H2O.
Đáp án: B
Câu 14: Chỉ ra nội dung sai khi nói về ion :
A. Ion là phần tử mang điện.
B. Ion âm gọi là cation, ion dương gọi là anion.
C. Ion có thể chia thành ion đơn nguyên tử và ion đa nguyên tử.
D. Ion được hình thành khi nguyên tử nhường hay nhận electron.
Đáp án: B
Câu 15: Liên kết hóa học giữa các ion được gọi là :
A. liên kết anion – cation.
B. liên kết ion hóa.
C. liên kết tĩnh điện.
D. liên kết ion.
Đáp án: A
Xem thêm các bài giải Trắc nghiệm Hóa lớp 10 Cánh diều hay, chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.