Toptailieu.vn biên soạn và giới thiệu cách viết Cấu hình electron của Be (beri), beryllium chương trình mới của ba bộ sách Kết nối tri thức, Cánh diều, Chân trời sáng tạo giúp học sinh dễ dàng nắm vững cách viết Cấu hình electron của Be (beri), beryllium từ đó học tốt môn Hóa học.
Nội dung bài viết
I. Cấu hình electron của Be (beri), beryllium chương trình mới
1. Cấu hình electron nguyên tử beryllium (Z = 4)
- Be có số hiệu nguyên tử là 4 ⇒ Nguyên tử Be có 4 electron.
- Cấu hình electron nguyên tử Be là 1s22s2.
Viết gọn: [He]2s2.
2. Cấu hình electron nguyên tử beryllium (Z = 4) theo ô orbital.
- Cấu hình electron nguyên tử beryllium (Z = 4) theo ô orbital là:
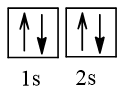
- Nguyên tử Be không có electron độc thân.
3. Mối liên hệ giữa cấu hình electron với vị trí trong bảng tuần hoàn và tính chất nguyên tố
- Vị trí Be trong bảng tuần hoàn:
Từ cấu hình electron của Be là 1s22s2 xác định được:
+ Be thuộc ô thứ 4 (do Z = 4).
+ Chu kì 2 (do có 2 lớp electron).
+ Nhóm IIA (do có 2 electron hóa trị, nguyên tố s).
+ Là nguyên tố s (do cấu hình electron lớp ngoài cùng là 2s2).
- Tính chất nguyên tố:
+ Be thuộc nhóm IIA ⇒ là kim loại kiềm thổ.
+ Be có 2 electron ở lớp ngoài cùng, có xu hướng nhường 2 electron này khi hình thành liên kết hóa học để đạt cấu hình bền vững của He ⇒ Be có tính khử.
+ Hóa trị cao nhất với oxygen = số thứ tự nhóm = II
+ Công thức oxide cao nhất: BeO (là oxide lưỡng tính)
+ Công thức hydroxide tương ứng: Be(OH)2 (là hydroxide lưỡng tính)
4. Bài tập
Câu 1: Nguyên tố R có cấu hình electron: 1s22s2. Công thức hợp chất oxide ứng với hóa trị cao nhất của R là
A. RO2
B. R2O5
C. RO
D. R2O
Lời giải:
Đáp án đúng là: C
Nguyên tố R có cấu hình electron: 1s22s2
⇒ R thuộc nhóm IIA.
⇒ Hóa trị cao nhất trong hợp chất oxide là II
⇒ Công thức hợp chất oxide ứng với hóa trị cao nhất của R là RO.
Câu 2: Nguyên tố Be thuộc ô số 4 trong bảng tuần hoàn. Cấu hình electron của nguyên tử nguyên tố Be là:
A. 1s2 2s2.
B. 1s2.
C. 1s2 2s23s1.
D. 1s2 2s23s2.
Lời giải:
Đáp án đúng là: A
Số thứ tự ô nguyên tố = số hiệu nguyên tử Z = số electron = 4
⇒ Cấu hình electron của nguyên tử Be là 1s2 2s2.
II. Cấu hình electron của Be (beri) chương trình cũ
1. Cấu hình electron nguyên tử beri (Z = 4)
- Beri có số hiệu nguyên tử là 4 ⇒ nguyên tử Be có 4 electron.
- Cấu hình electron nguyên tử beri là 1s2 2s2.
Viết gọn: [He]2s2.
2. Mối quan hệ giữa cấu hình electron với vị trí trong bảng tuần hoàn và tính chất nguyên tố
- Vị trí Be trong bảng tuần hoàn:
+ Từ cấu hình electron của Be 1s2 2s2 xác định được nguyên tử Be có 4 electron, phân bố trên 2 lớp electron và số electron lớp ngoài cùng bằng 2.
⇒ Vậy beri ở ô thứ 4 (do Z = 4); chu kì 2 (do có 2 lớp electron), nhóm IIA (do có 2 electron hóa trị, nguyên tố s).
- Tính chất nguyên tố:
+ Beri có 2 electron ở lớp ngoài cùng nên Be là kim loại.
+ Beri có xu hướng nhường 2 electron khi tham gia phản ứng hóa học để đạt cấu hình bền vững của He.
+ Công thức oxit: BeO (là oxit lưỡng tính)
+ Công thức bazơ tương ứng: Be(OH)2 (là hiđroxit lưỡng tính)
3. Bài tập
Câu 1: Nguyên tố Y chỉ có electron điền vào phân lớp s. Y thuộc chu kì mấy? (Biết rằng Y thuộc nhóm IIA)
A. Chu kì 1
B. Chu kì 2
C. Chu kì 3
D. Chu kì 4
Lời giải:
Đáp án B
Nguyên tố Y chỉ có electron điền vào phân lớp s
⇒ Y thuộc chu kì 1 hoặc chu kì 2
Mà Y thuộc nhóm IIA nên Y thuộc chu kì 2.
Câu 1: Nguyên tố X ở chu kì 2, nhóm IIA có cấu hình electron là
A. 1s2 2s2.
B. 1s2.
C. 1s2 2s23s1.
D. 1s2 2s23s2.
Lời giải:
Đáp án A
Nguyên tố X ở chu kì 2, nhóm IIA
⇒ Nguyên tử X có 2 lớp electron và có 2 electron lớp ngoài cùng.
⇒ Cấu hình electron của nguyên tử X là 1s2 2s2.
Xem thêm các bài giải Cấu hình electron của các nguyên tố chương trình mới hay, chi tiết khác:
Cấu hình electron của H, hydrogen (hiđro) chương trình mới
Cấu hình electron của He, helium (heli) chương trình mới
Cấu hình electron của Li, lithium (liti) chương trình mới
Cấu hình electron của Be, beryllium (beri) chương trình mới
Cấu hình electron của B, boron (bo) chương trình mới
Cấu hình electron của C, carbon (cacbon) chương trình mới
Cấu hình electron của N, nitrogen (nitơ) chương trình mới
Cấu hình electron của O, oxygen (oxi) chương trình mới
Cấu hình electron của F, fluorine (flo) chương trình mới
Cấu hình electron của Ne, neon chương trình mới
Cấu hình electron của Na, sodium (natri) chương trình mới
Cấu hình electron của Mg, magnesium (magie) chương trình mới
Cấu hình electron của Al, aluminium (nhôm) chương trình mới
Cấu hình electron của Si, silicon (silic) chương trình mới
Cấu hình electron của P, phosphorus (photpho) chương trình mới
Cấu hình electron của S, sulfur (lưu huỳnh) chương trình mới
Cấu hình electron của Cl, chlorine (clo) chương trình mới
Cấu hình electron của Ar, argon (agon) chương trình mới
Cấu hình electron của K, potassium (kali) chương trình mới
Cấu hình electron của Ca, calcium (canxi) chương trình mới
Cấu hình electron của Cr, chromium (crom) chương trình mới
Cấu hình electron của Ba, barium (bari) chương trình mới
Cấu hình electron của Co, cobalt (coban) chương trình mới
Cấu hình electron của Cu, copper (đồng) chương trình mới
Cấu hình electron của Au, gold (vàng) chương trình mới
Cấu hình electron của Mn, manganese (mangan) chương trình mới
Cấu hình electron của Ag, silver (bạc) chương trình mới
Cấu hình electron của Sr, strontium (stronti) chương trình mới
Cấu hình electron của Ti, titanium (titan) chương trình mới
Cấu hình electron của V, vanadium (vanadi) chương trình mới
Cấu hình electron của Xe, xenon chương trình mới
Cấu hình electron của Zn, zinc (kẽm) chương trình mới
Cấu hình electron của Fe, iron (sắt) chương trình mới
Cấu hình electron của Ni, nickel (niken) chương trình mới
Cấu hình electron của Rb, rubidium (rubidi) chương trình mới
Cấu hình electron nguyên tử của các nguyên tố thường gặp chương trình mới
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.