Toptailieu.vn biên soạn và giới thiệu phương trình phản ứng Mg + HCl → MgCl2 + H2 | Mg ra MgCl2. Phản ứng Mg + HCl → MgCl2 + H2 | Mg ra MgCl2 thuộc loại phản ứng oxi hóa khử, phản ứng thế đã được cân bằng chính xác và chi tiết nhất. Bài viết giới thiệu các nội dung liên quan giúp học sinh nắm bắt kiến thức cơ bản. Mời các bạn đón đọc:
Nội dung bài viết
1. Phương trình phản ứng hóa học:
Mg + 2HCl → MgCl2 + H2
2. Hiện tượng nhận biết phản ứng
Magie tan trong dung dịch HCl tạo dung dịch không màu.
3. Điều kiện phản ứng
Không điều kiện
4. Tính chất hóa học
- Magie là chất khử mạnh:
Mg → Mg2+ + 2e
a. Tác dụng với phi kim
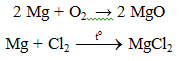
Lưu ý:
- Do Mg có ái lực lớn với oxi: 2Mg + CO2 → MgO. Vì vậy không dùng tuyết cacbonic để dập tắt đám cháy Mg.
b. Tác dụng với axit
- Với dung dịch HCl và H2SO4 loãng:
Mg + H2SO4 → MgSO4 + H2
- Với dung dịch HNO3:
4Mg + 10 HNO3 → 4 Mg(NO3)2 + NH4NO3 + 3 H2O
5. Cách thực hiện phản ứng
Cho magie tác dụng với dung dịch HCl thu được muối và khí không màu thoát ra.
6. Bạn có biết
Mg dễ tham gia phản ứng với các dung dịch axit không có tính oxi hóa tạo muối và khí hidro thoát ra.
7. Bài tập liên quan
Ví dụ 1: Dãy nào sau đây chỉ gồm các chất vừa tác dụng được với dung dịch HCl, vừa tác dụng được với dung dịch AgNO3 ?
A. Fe, Ni, Ag
B. Zn, Cu, Mg
C. Cu, Na, Ba
D. Cr, Fe, Al
Hướng dẫn giải:
Đáp án D
Cr + 2HCl → CrCl2 + H2
Fe + 2HCl →FeCl2 + H2
2Al + 6HCl → 2AlCl3 + 3H2
Cr + 2AgNO3 → Cr(NO3)2 + 2Ag
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Al + 3AgNO3 → Al(NO3)3 + 3Ag
Ví dụ 2: Hòa tan hoàn toàn 15,4 gam hỗn hợp Mg và Zn trong dung dịch HCl dư thấy có 0,6 gam khí H2 bay ra. Khối lượng muối tạo thành trong dung dịch là
A. 35,7 gam
B. 36,7 gam
C. 53,7gam
D. 63,7 gam
Hướng dẫn giải:
Đáp án B
nCl- = nHCl = 2nH2 = 0,6 mol.
Ta có: mmuối = mKL + 35,5. nCl-
⇒ mmuối = 36,7 gam.
Ví dụ 3: Cấu hình e nào dưới đây đúng với Mg
A. 1s22s22p63s2
B. 1s22s22p63s23p2
C. 1s22s22p6
D. 1s22s22p63s23p3
Hướng dẫn giải:
Đáp án A
Bài viết cùng bài học:




