Toptailieu.vn biên soạn và giới thiệu phương trình phản ứng Al2S3 + SiO2 → Al2O3 + SiS2 | Al2S3 ra Al2O3 . Đây là phản ứng trao đổi đã được cân bằng chính xác và chi tiết nhất. Bài viết giới thiệu các nội dung liên quan giúp
Nội dung bài viết
1. Phương trình phản ứng hóa học:
2Al2S3 + 3SiO2 → 2Al2O3 + 3SiS2
2. Hiện tượng nhận biết phản ứng
- Phản ứng tạo thành nhôm oxit và silic đisunfua
3. Điều kiện phản ứng
- Nhiệt độ: 1200 - 1300oC
4. Tính chất hoá học
a. Tính chất hoá học của Al2S3
- Tác dụng với nước
Al2S3 + H2O → Al(OH)3 + H2S
- Tác dụng với axit
Al2S3 + HCl → AlCl3 + H2S
- Tác dụng với dung dịch bazo
Al2S3 + NaOH → Al(OH)3 + Na2S
- Tác dụng với dung dịch muối
Al2S3 + Cu(NO3)2 → Al(NO3)3 + CuS
b. Tính chất hoá học của SiO2
- SiO2 là oxit axit.
- Silic đioxit không phản ứng với nước.
- Ở nhiệt độ cao, tác dụng với kiềm và oxit bazơ tạo thành muối silicat. Ví dụ:
SiO2 + 2NaOH 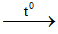
SiO2 + CaO 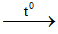
5. Cách thực hiện phản ứng
- Cho Al2S3 tác dụng với SiO2
6. Bài tập liên quan
Ví dụ 1: Dãy gồm các oxit đều bị Al khử ở nhiệt độ cao là:
A. PbO, K2O, SnO.
B. FeO, MgO, CuO.
C. Fe3O4, SnO, BaO.
D. FeO, CuO, Cr2O3.
Đáp án: D
Hướng dẫn giải
Phản ứng nhiệt nhôm là để khử các oxit kim loại đứng sau Al trong dãy điện hóa. Vậy các oxit thỏa mãn điều kiện trên là: PbO, SnO, FeO, CuO, Fe3O4, Cr2O3.
Ví dụ 2: Cho các quặng sau: pirit, thạch cao, mica, apatit, criolit, boxit, dolomit. Số quặng chứa nhôm là:
A. 2.
B. 3.
C. 4.
D. 5.
Đáp án: B
Hướng dẫn giải
Cryolit: Na3AlF6 hay AlF3.3NaF
Boxit: Al2O3.nH2O
Mica: K2O.Al2O3.6SiO2.2H2O
Ví dụ 3: Cho sơ đồ phản ứng: Al → X → Al2O3 → Al
X có thể là
A. AlCl3.
B. NaAlO2.
C. Al(NO3)3.
D. Al2(SO4)3.
Đáp án: C
học sinh nắm bắt kiến thức cơ bản. Mời các bạn đón đọc:
Bài viết cùng bài học:




