Toptailieu.vn biên soạn và giới thiệu phương trình phản ứng CuO + Al → Cu + Al2O3 | CuO ra Cu . Đây là phản ứng oxi hóa khử, phản ứng nhiệt nhôm đã được cân bằng chính xác và chi tiết nhất. Bài viết giới thiệu các nội dung liên quan giúp học sinh nắm bắt kiến thức cơ bản. Mời các bạn đón đọc:
Nội dung bài viết
1. Phương trình phản ứng hóa học:
3CuO + 2Al → 3Cu + Al2O3
2. Hiện tượng nhận biết phản ứng
- Bột CuO màu đen chuyển dần sang màu đỏ gạch là Cu.
3. Điều kiện phản ứng
- Nhiệt độ cao.
4. Tính chất hoá học
- Có đầy đủ tính chất hóa học của một oxit bazơ.
- Dễ bị khử về kim loại đồng.
Tác dụng với axít
CuO + 2HCl → CuCl2 + H2O
CuO + 2HNO3 → Cu(NO3)2 + H2O
Tác dụng với oxit axit
3CuO + P2O5 → Cu3(PO4)2
Tác dụng với các chất khử mạnh: H2, C, CO...
H2 + CuO 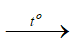 H2O + Cu
H2O + Cu
CO + CuO 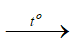 CO2 + Cu
CO2 + Cu
5. Cách thực hiện phản ứng
- Trộn bột nhôm với bột CuO màu đen rồi đun nóng.
6. Bạn có biết
Tương tự các oxit bazơ đứng sau oxit nhôm trong dãy hoạt động hóa học (như FeO, PbO….) có phản ứng nhiệt nhôm.
7. Bài tập liên quan
Ví dụ 1: Dãy gồm các oxit đều bị Al khử ở nhiệt độ cao là:
A. PbO, K2O, SnO.
B. FeO, MgO, CuO.
C. Fe3O4, SnO, BaO.
D. FeO, CuO, Cr2O3.
Đáp án D
Hướng dẫn giải:
- Phản ứng nhiệt nhôm là phản ứng hóa học tỏa nhiệt trong đó nhôm là chất khử ở nhiệt độ cao. Phương pháp này dùng để khử các oxit kim loại đứng sau Al trong dãy điện hóa.
Vậy các oxit thỏa mãn điều kiện trên là: PbO, SnO, FeO, CuO, Fe3O4, Cr2O3.
Ví dụ 2: Khử 16g bột Fe2O3 bằng m(g) bột Al vừa đủ. Giá trị của m là
A. 2,7g
B. 5,4g
C. 3,2g
D. 6,4g
Đáp án B
Hướng dẫn giải:
Fe2O3 + 2Al → 2Fe + Al2O3
nFe2O3 = 0,1mol ⇒ nAl = 0,2mol ⇒ mAl = 5,4g
Ví dụ 3: Trộn 5,4g bột Al với 4,8g CuO rồi thực hiện phản ứng nhiệt nhôm thu được m gam chất rắn. Giá trị của m là
A. 10,2g
B. 4,08g
C. 2,24g
D. đáp án khác
Đáp án A
Hướng dẫn giải:
nAl = 0,2mol; nCuO = 0,06 mol
2Al + 3CuO → Al2O3 + 3Cu
Bđ 0,2 0,06
Pư 0,04 0,06 0,02 0,06
Dư 0,16 0
m = mAl dư + mAl2O3 + mCu = 0,16.27 + 0,02.102 + 0,06.64 = 10,2g.
Bài viết cùng bài học:




