Toptailieu.vn biên soạn và giới thiệu phương trình phản ứng Fe(OH)2 + H2SO4 → H2O + FeSO4 | Fe(OH)2 ra FeSO4. Đây là phản ứng trao đổi đã được cân bằng chính xác và chi tiết nhất. Bài viết giới thiệu các nội dung liên quan giúp học sinh nắm bắt kiến thức cơ bản. Mời các bạn đón đọc:
Nội dung bài viết
1. Phương trình phản ứng hóa học
Fe(OH)2 + H2SO4 → 2H2O + FeSO4
2. Hiện tượng nhận biết phản ứng
- Chất rắn màu trắng xanh Fe(OH)2 tan dần trong dung dịch
3. Điều kiện phản ứng
- Nhiệt độ phòng.
4. Tính chất hoá học
4.1. Tính chất hoá học của Fe(OH)2
- Có tính chất của bazo không tan.
- Vừa có tính oxi hóa vừa có tính khử.
Bị nhiệt phân
- Nung Fe(OH)2 trong điều kiện không có không khí
Fe(OH)2 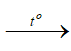 FeO + H2O
FeO + H2O
- Nung Fe(OH)2 trong không khí
4Fe(OH)2 + O2 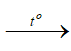 2Fe2O3 + 4H2O
2Fe2O3 + 4H2O
Tác dụng với axit
- Với axit không có tính oxi hóa như (HCl, H2SO4)
Fe(OH)2 + 2HCl → FeCl2 + 2H2O
Tính khử:
- Với axit HNO3, H2SO4 đặc
3Fe(OH)2 + 10HNO3 loãng → 3Fe(NO3)3 + NO + 8H2O
2Fe(OH)2 + 4H2SO4 → Fe2(SO4)3 + SO2 + 4H2O
- Tác dụng với các chất oxi hóa khác
4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3
4.2. Tính chất hoá học của H2SO4
Axit sunfuric loãng
- Axit sunfuric là một axit mạnh, hóa chất này có đầy đủ các tính chất hóa học chung của axit như:
- Axit sunfuric H2SO4 làm chuyển màu quỳ tím thành đỏ.
- Tác dụng với kim loại đứng trước H (trừ Pb)
Fe + H2SO4 → FeSO4 + H2
- Tác dụng với oxit bazo
FeO + H2SO4 → FeSO4 + H2O
- Tác dụng với bazo
H2SO4 + NaOH → NaHSO4 + H2O
H2SO4 + 2NaOH → Na2SO4 + 2H2O
- Tác dụng với muối
Na2CO3 + H2SO4 → Na2SO4 + H2O + CO2
H2SO4 + 2KHCO3 → K2SO4 + 2H2O + 2CO2
Axit sunfuric đặc
- Axit sunfuric đặc có tính axit mạnh, oxi hóa mạnh với tính chất hóa học nổi bật như:
- Tác dụng với kim loại:
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
- Tác dụng với phi kim
C + 2H2SO4 → CO2 + 2H2O + 2SO2 (nhiệt độ)
2P + 5H2SO4 → 2H3PO4 + 5SO2 + 2H2O
- Tác dụng với các chất khử khác.
2FeO + 4H2SO4 → Fe2(SO4)3 + SO2 + 4H2O
- H2SO4 còn có tính háo nước đặc trưng
C12H22O11 + H2SO4 → 12C + H2SO4.11H2O
5. Cách thực hiện phản ứng
- Cho Fe(OH)2 tác dụng với dung dịch H2SO4
6. Bạn có biết
Tương tự Fe(OH)2 các hidroxit phản ứng với axit tạo thành muối và nước
7. Bài tập liên quan
Ví dụ 1: Phản ứng nào sau đây xảy ra:
A. Fe + CuSO4 → FeSO4 + Cu
B. Fe + ZnSO4 → FeSO4 + Zn
C. 2Fe + 3CuSO4 → Fe2(SO4)3 + 3Cu
D. 2Ag + Fe(NO3)2 → 2AgNO3 + Fe
Hướng dẫn giải
Kim loại đứng trước trong dãy hoạt động hóa học sẽ đẩy được muối của kim loại đứng sau ra khỏi dung dịch.
Đáp án : A
Ví dụ 2: Để tách Ag ra khỏi hỗn hợp Ag, Cu, Fe mà khối lượng Ag không thay đổi thì dùng chất nào sau đây ?
A. FeSO4
B. CuSO4
C. Fe2(SO4)3
D. AgNO3
Hướng dẫn giải
Fe + Fe2(SO4)3 → 3FeSO4
Cu + Fe2(SO4)3 → 3FeSO4 + CuSO4
Đáp án : C
Ví dụ 3: Dung dịch FeSO4 không làm mất màu dung dịch nào sau đây ?
A. Dung dịch KMnO4 trong môi trường H2SO4
B. Dung dịch K2Cr2O7 trong môi trường H2SO4
C. Dung dịch Br2
D. Dung dịch CuCl2
Hướng dẫn giải
KMnO4, K2Cr2O7, Br2 đều có tính oxi hóa mạnh nên đều tác dụng với Fe2+
Đáp án : D
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.