Toptailieu.vn biên soạn và giới thiệu phương trình phản ứng 2KOH + CO2 → K2CO3 + H2O | KOH ra K2CO3 . Phản ứng 2KOH + CO2 → K2CO3 + H2O | KOH ra K2CO3 thuộc loại phản ứng trao đổi đã được cân bằng chính xác và chi tiết nhất. Bài viết giới thiệu các nội dung liên quan giúp học sinh nắm bắt kiến thức cơ bản. Mời các bạn đón đọc:
Nội dung bài viết
1. Phương trình phản ứng hóa học:
2KOH + CO2 → K2CO3 + H2O
2. Hiện tượng nhận biết phản ứng
- Quan sát sự chuyển màu của chỉ thị phù hợp trước và sau phản ứng.
3. Điều kiện phản ứng
- Phản ứng xảy ra ngay điều kiện thường.
4. Tính chất hóa học
- KOH là một bazo mạnh có khả năng làm thay đổi màu sắc các chất chỉ thị như khiến quỳ tím chuyển sang màu xanh, còn dung dịch phenolphtalein không màu thành màu hồng.
Ở điều kiện nhiệt độ phòng, KOH tác dụng với oxit axit như SO2, CO2
KOH + SO2 → K2SO3 + H2O
KOH + SO2 → KHSO3
- KOH tác dụng với axit tạo thành muối và nước
KOH(dd) + HCl(dd) → KCl(dd) + H2O
- KOH tác dụng với các axit hữu cơ để tạo thành muối và thủy phân este, peptit
RCOOR1 + KOH → RCOOK + R1OH
- KOH tác dụng với kim loại mạnh tạo thành bazo mới và kim loại mới
KOH + Na → NaOH + K
- KOH tác dụng với muối để tạo thành muối mới và axit mới
2KOH + CuCl2 → 2KCl + Cu(OH)2↓
- KOH là một bazo mạnh, trong nước phân ly hoàn toàn thành ion Na+ và OH-
Phản ứng với một số oxit kim loại mà oxit, hidroxit của chúng lưỡng tính như nhôm, kẽm,…
2KOH + 2Al + 2H2O → 2KAlO2 + 3H2↑
2KOH + Zn → K2ZnO2 + H2↑
- KOH phản ứng với một số hợp chất lưỡng tính
KOH + Al(OH)3 → KAlO2 + 2H2O
2KOH + Al2O3 → 2KAlO2 + H2O
5. Cách thực hiện phản ứng
- Dẫn khí CO2 vào ống nghiệm chứa KOH và vài giọt chất chỉ thị.
6. Bạn có biết
- KOH phản ứng với CO2 tùy theo tỉ lệ về số mol mà sản phẩm thu được có thể là muối cabonat trung hòa hoặc muối axit hoặc hỗn hợp cả hai muối.
- KOH phản ứng với CO2 chỉ thu được muối K2CO3 khi T = 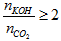 .
.
7. Bài tập liên quan
Ví dụ 1: Cho 2,24 lít khí CO2 ở đktc phản ứng với lượng dư dung dịch KOH thu được dung dịch X. Khối lượng muối tan có trong X là
A. 13,8 gam.
B. 12,8 gam.
C. 11,8 gam.
D. 10,8 gam.
Hướng dẫn giải
Do KOH dư nên có phản ứng
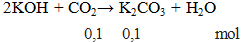
mmuối = 0,1.138 = 13,8 gam.
Đáp án A.
Ví dụ 2: Cho CO2 tác dụng với lượng dư dung dịch KOH thu được dung dịch X. Chất tan có trong dung dịch X là
A. K2CO3.
B. K2CO3 và KHCO3.
C. KHCO3.
D. K2CO3 và KOH.
Hướng dẫn giải
Do KOH dư nên có phản ứng
2KOH + CO2 → K2CO3 + H2O
Chất tan có trong dung dịch X là K2CO3 và KOH dư.
Đáp án D.
Ví dụ 3: Cho 2,24 lít khí CO2 ở đktc phản ứng với dung dịch chứa 0,3 mol KOH. Khối lượng muối tan có trong dung dịch sau phản ứng là
A. 13,8 gam.
B. 12,8 gam.
C. 11,8 gam.
D. 10,8 gam.
Hướng dẫn giải
Có T = 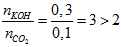 nên có phản ứng
nên có phản ứng
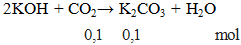
mmuối = 0,1.138 = 13,8 gam.
Đáp án A.
Ví dụ 4: Cho 3,36 lít khí CO2 tác dụng với 200 ml dung dịch KOH 1M. Xác định sản phẩm thu được sau khi kết thúc phản ứng.
A. K2CO3
B. KHCO3
C. K2CO3 và KHCO3
D. Không tạo ra sản phẩm
Đáp án C
Hướng dẫn giải
nCO2 = 3,36/22,4 = 0,15 mol
nKOH = 0,2 mol
Xét tỉ lệ T = nKOH/nCO2 = 0,2/0,15 = 1,3
1 < 1,3 < 2 : tạo cả muối KHCO3 và K2CO3
Ví dụ 5: Cho 2,24 lít khí CO2 tác dụng với 100 ml dung dịch KOH 1M. Xác định sản phẩm thu được sau khi kết thúc phản ứng thu được m gam muối. Tính khối lượng muối thu được.
A. 10 gam
B. 12 gam
C. 20 gam
D. 15 gam
Đáp án A
Hướng dẫn giải
nCO2 = 2,24/22,4 = 0,1 mol
nKOH = 0,1 mol
Xét tỉ lệ T = nKOH/nCO2 = 0,1/0,1 = 1
Nếu T = 1 : chỉ tạo muối KHCO3
CO2 + KOH → KHCO3 (2)
nKHCO3 = nCO2 = 0,1 mol => mKHCO3 = 0,1.100 = 10 gam
Ví dụ 6: Để nhận biết 2 khí CO2 và SO2 người ta sử dụng hóa chất nào sau đây?
A. dung dịch nước vôi trong
B. quỳ tím
C. dung dịch NaNO3
D. dung dịch brom
Đáp án D
Hướng dẫn giải
Để phân biệt được hai loại khí này người ta thường sử dụng các loại thuốc thử có tính oxi hóa mạnh như thuốc tím (KMnO4) hoặc dung dịch Brom (Br2).
Khí SO2 còn có thể làm mất màu dung dịch Brom:
Br2 + SO2 + 2H2O → H2SO4 + 2HBr
Ví dụ 7: Cặp chất nào dưới đây có thể tồn tại trong cùng 1 dung dịch
A. NaCl; AgNO3
B. Ba(NO3)2, H2SO4
C. KOH; CuCl2
D. NaCl; HCl
Đáp án D
Hướng dẫn giải
Cặp chất có thể tồn tại trong cùng 1 dung dịch là cặp chất không phản ứng với nhau
NaCl + AgNO3 → AgCl + NaNO3
Ba(NO3)2 + H2SO4 → BaSO4 + 2HNO3
2KOH + CuCl2 → Cu(OH)2 + 2KCl
NaCl không tác dụng với HCl
Ví dụ 8: Dãy các chất tác dụng được với dung dịch H2SO4 loãng tạo thành sản phẩm có chất khí là
A. Na2SO3, CaCO3, Zn.
B. Al, MgO, KOH.
C. BaO, Fe, CaCO3.
D. Zn, Fe2O3, Na2SO3.
Đáp án A
Hướng dẫn giải
Na2SO3 + H2SO4 → Na2SO4 + SO2 + H2O
CaCO3 + H2SO4 → CaSO4 + CO2 + H2O
Zn + H2SO4 → ZnSO4 + H2
2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑
H2SO4 + MgO → H2O + MgSO4
H2SO4 + 2KOH → 2H2O + K2SO4
→ Loại vì có 2 phản ứng với MgO và KOH không sinh ra khí
C.
BaO + H2SO4 → H2O + BaSO4
Fe + H2SO4 → H2 + FeSO4
CaCO3 + H2SO4 → H2O + CO2 + CaSO4
→ Loại vì có 2 phản ứng với BaO không sinh ra khí
D.
H2SO4 + Zn → H2 + ZnSO4
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
Na2SO3 + H2SO4 → Na2SO4 + SO2 + H2O
→ Loại vì có phản ứng với Fe2O3 không sinh ra khí
Ví dụ 9: Dãy chất nào sau đây gồm các bazơ không bị nhiệt phân hủy?
A. Mg(OH)2, Ba(OH)2, Fe(OH)2
B. NaOH, Ba(OH)2, Al(OH)3
C. KOH, Ca(OH)2, LiOH
D. Zn(OH)2, Al(OH)3, Cu(OH)2
Đáp án C
Hướng dẫn giải
A. sai do có Mg(OH)2, Fe(OH)2 bị nhiệt phân hủy
Mg(OH)2 → MgO + H2O ↑
4Fe(OH)2 + O2 → 4Fe(OH)2 + O2
B. sai do có Al(OH)3 bị phân hủy
2Al(OH)3 → Al2O3 + 3H2O
C. đúng
D.
Zn(OH)2 → ZnO + H2O ↑
Cu(OH)2→ CuO + H2O ↑
2Al(OH)3 → Al2O3 + 3H2O
Ví dụ 10: Cặp dung dịch nào sau đây phản ứng với nhau tạo ra chất khí?
A. NH4Cl và AgNO3.
B. KOH và H2SO4.
C. Ba(OH)2 và NH4Cl.
D. Na2CO3và KOH.
Đáp án C
Hướng dẫn giải
A. NH4Cl + AgNO3 → AgCl ↓ + NH4NO3
B. 2KOH + H2SO4 → K2SO4 + 2H2O
C. Ba(OH)2 + 2NH4Cl → BaCl2 + 2NH3 ↑ + 2H2O
D. Na2CO3 không phản ứng với KOH
Ví dụ 11: Sục khí CO2 vào dung dịch nước vôi trong, hiện tượng xảy ra:
A. Có kết tủa ngay, lượng kết tủa tăng dần qua một cực đại rồi sau đó tan trở lại hết.
B. Một lúc mới có kết tủa, lượng kết tủa tăng dần qua một cực đại rồi lại giảm.
C. Có kết tủa ngay, nhưng kết tủa tan trở lại ngay sau khi xuất hiện.
D. Có kết tủa ngay, lượng kết tủa tăng dần đến một giá trị không đổi.
Đáp án A
Hướng dẫn giải
Hiện tượng: Ban đầu xuất hiện kết tủa trắng, sau đó kết tủa trắng tan dần tạo dung dịch trong suốt.
Phương trình hóa học: CO2 + Ca(OH)2 → CaCO3 ↓ trắng + H2O
CO2 + CaCO3 + H2O → Ca(HCO3)2
Ví dụ 12: Thổi V lít khí CO2 (đktc) vào 200ml dung dịch Ca(OH)21M thu được 12 gam kết tủa. Lọc kết tủa đun nóng dd lại thấy có kết tủa nữa. Tìm V?
A. 3,136 lít
B. 6,272 lít
C. 4,181 lít
D. 7,840 lít
Đáp án B
Hướng dẫn giải
nCaCO3 = 12/100 = 0,12 mol
nCa(OH)2 = 0,2 mol
Do đun nóng lại thu được thêm kết tủa => nên có Ca(HCO3)2
nCaCO3 tạo thêm là 8/100 = 0,08 mol
Phương trình hóa học
CO2+ Ca(OH)2 → CaCO3+ H2O
0,12 → 0,12 → 0,12
2CO2+ Ca(OH)2 → Ca(HCO3)2
Ca(HCO3)2→ CaCO3 + CO2 + H2O
0,08 → 0,08
→ nCO2 ở phản ứng 2 là 0,08.2 = 0 ,16 mol
→ nCO2= 0,12 + 0,16 = 0,28 mol
→ V = 0,28.22,4 = 6,272 lít
Ví dụ 13: Cho các dung dịch: NaOH, NaCl, H2SO4, Na2SO4, Ba(OH)2. Chỉ dùng thêm một thuốc thử nào sau đây để nhận biết?
A. Phenolphtalein.
B. Quỳ tím.
C. BaCl2.
D. AgNO3.
Đáp án B
Hướng dẫn giải
Dùng quỳ tím nhận biết được dung dịch NaOH làm quỳ tím chuyển sang màu xanh, dung dịch H2SO4 làm quỳ tím chuyển sang màu đỏ.
Sau đó cho dùng dung dịch H2SO4 vừa nhận vào 3 mẫu còn lại;
Xuất hiện kết tủa trắng là Ba(OH)2
Ba(OH)2 + H2SO4 → BaSO4 + H2O
Không hiện tượng là NaCl và Na2SO4
Cho dung dịch Ba(OH)2 vừa nhận biết đc vào 2 mẫu còn lại:
Xuất hiện kết tủa trắng là Na2SO4
Na2SO4 + Ba(OH)2 → NaOH + BaSO4
Xem thêm Một số phương trình phản ứng hóa học khác của Kali (K) & Hợp chất, chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.