Toptailieu.vn biên soạn và giới thiệu phương trình phản ứng Cr + S → Cr2S3 | Cr ra Cr2S3. Đây là phản ứng oxi hóa khử, phản ứng hóa hợp đã được cân bằng chính xác và chi tiết nhất. Bài viết giới thiệu các nội dung liên quan giúp học sinh nắm bắt kiến thức cơ bản. Mời các bạn đón đọc
Nội dung bài viết
1. Phương trình phản ứng hóa học:
2Cr + 3S → Cr2S3
2. Hiện tượng nhận biết phản ứng
- Khi cho hỗn hợp bột Cr và bột S đốt trên ngọn lửa đèn cồn thì thấy hiện tượng cháy sáng.
3. Điều kiện phản ứng
- Nhiệt độ cao.
4. Tính chất hoá học
4.1. Tính chất hoá học của Crom
- Là kim loại có tính khử mạnh hơn sắt.
- Trong các hợp chất crom có số oxi hoá từ +1 → +6 (hay gặp +2, +3 và +6).
Tác dụng với phi kim
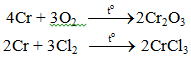
Tác dụng với nước
Cr bền với nước và không khí do có lớp màng oxit rất mỏng, bền bảo vệ. Người ta mạ crom lên sắt để bảo vệ sắt và dùng Cr để chế tạo thép không gỉ.
Tác dụng với axit
Cr + 2HCl → CrCl2 + H2
Cr + H2SO4 → CrSO4 + H2
Cr không tác dụng với dung dịch HNO3 hoặc H2SO4 đặc, nguội.
4.2. Tính chất hoá học của Lưu huỳnh (S)
Tác dụng với kim loại và hidro
Lưu huỳnh thể hiện tính oxi hóa khi tác dụng với kim loại và hidro.
- Tác dụng với hiđro:
H2 + S → H2S (350oC)
- Tác dụng với kim loại (có to, tạo sản phẩm có số oxh thấp của kim loại).
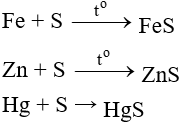
(Thủy phân sunfua, phản ứng xảy ra ở nhiệt độ thường nên thường dùng S khử độc Hg)
Chú ý: Một số muối sunfua có màu đặc trưng: CuS, PbS, Ag2S (màu đen); MnS (màu hồng); CdS (màu vàng) → thường được dùng để nhận biết gốc sunfua.
- Muối sunfua được chia thành 3 loại:
+ Loại 1. Tan trong nước gồm Na2S, K2S, CaS và BaS, (NH4)2S.
+ Loại 2. Không tan trong nước nhưng tan trong axit mạnh gồm FeS, ZnS, ...
+ Loại 3. Không tan trong nước và không tan trong axit gồm CuS, PbS, HgS, Ag2S, ...
Tác dụng với phi kim và hợp chất
S thể hiện tính khử khi tác dụng với 1 số phi kim và 1 số hợp chất có tính oxi hóa.
- Tác dụng với oxi:
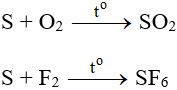
- Tác dụng với các chất có tính oxi hóa mạnh:
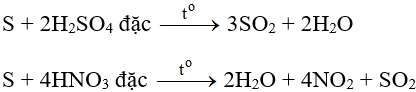
5. Cách thực hiện phản ứng
- Trộn bột crom với bột lưu huỳnh và đốt cháy trên ngọn lửa đèn cồn.
6. Bạn có biết
- Ở nhiệt độ cao crom cũng khử được nhiều phi kim trừ flo.
7. Bài tập liên quan
Ví dụ 1: Ở nhiệt độ thường, crom chỉ tác dụng với
A. flo
B. clo
C. oxi
D. lưu huỳnh
Hướng dẫn giải
Đáp án A
Ví dụ 2: Chọn phát biểu đúng về phản ứng của crom với phi kim?
A. Ở nhiệt độ thường, crom chỉ phản ứng với flo.
B. Ở nhiệt độ cao, oxi oxi hóa crom tạo thành Cr(VI).
C. Lưu huỳnh không phản ứng được với crom.
D. Ở nhiệt độ cao, clo sẽ oxi hóa crom thành Cr(II).
Hướng dẫn giải
Đáp án A
Ví dụ 3: Phản ứng nào sau đây không đúng ?
A. Cr + 2F2 → CrF4
B. 2Cr + 3Cl2 → 2CrCl3
C. 2Cr + 3S → Cr2S3
D. 6Cr + 3N2 → 6CrN
Hướng dẫn giải
Đáp án A
Giải thích:
Các phản ứng B, C, D đúng.
Đáp án A sai vì 2Cr + 3F2 → 2CrF3
Xem thêm Một số phương trình phản ứng hóa học khác của Crom (Cr) & Hợp chất, chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.