Toptailieu.vn biên soạn và giới thiệu phương trình phản ứng Mn + Cl2 → MnCl2 | Mn ra MnCl2. Đây là phản ứng oxi hóa khử đã được cân bằng chính xác và chi tiết nhất. Bài viết giới thiệu các nội dung liên quan giúp học sinh nắm bắt kiến thức cơ bản. Mời các bạn đón đọc:
Nội dung bài viết
1. Phương trình phản ứng hóa học:
Mn + Cl2 → MnCl2
2. Hiện tượng nhận biết phản ứng
Mangan cháy trong Clo tạo muối màu đỏ nhạt
3. Điều kiện phản ứng
Nhiệt độ gần 200°C
4. Tính chất hoá học
a. Tính chất hoá học của Mangan
- Trạng thái ôxi hóa phổ biến của nó là +2, +3, +4, +6 và +7. Trạng thái ôxy hóa ổn định nhất là mangan +2.
- Mangan có tính khử khá mạnh
Tác dụng với phi kim
- Tác dụng trực tiếp được với nhiều phi kim.
Mn (bột) + O2→ MnO2. (tự bốc cháy)
Mn + Cl2 → MnCl2.
Tác dụng với axit
- Tác dụng với HCl và H2SO4 loãng:
Mn (bột) + 2HCl (loãng) → MnCl2 + H2
- Tác dụng với HNO3 và H2SO4 đặc:
Mn + 2H2SO4 (đặc) → MnSO4 + SO2 + 2H2O.
3Mn + 8HNO3 (loãng, nóng) → 3Mn(NO3)2 + 2NO + 4H2O.
Tác dụng với nước
Mn (bột) + 2H2O (hơi) → Mn(OH)2 + H2
b. Tính chất hoá học của Cl2
Tác dụng với kim loại
Đa số kim loại và có to để khơi màu phản ứng tạo muối clorua (có hoá trị cao nhất )
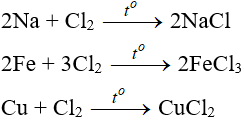
Tác dụng với phi kim
(cần có nhiệt độ hoặc có ánh sáng)
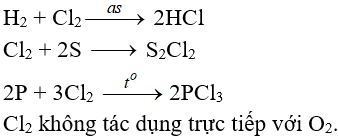
Tác dụng với nước và dung dịch kiềm
Cl2 tham gia phản ứng với vai trò vừa là chất ôxi hóa, vừa là chất khử.
Tác dụng với nuớc
Khi hoà tan vào nước, một phần Clo tác dụng (Thuận nghịch)
Cl20 + H2O → HCl + HClO (Axit hipoclorơ)
Axit hipoclorơ có tính oxy hoá mạnh, nó phá hửy các màu vì thế nước clo hay clo ẩm có tính tẩy màu do.
Tác dụng với muối của các halogen khác
Cl2 + 2NaBr → 2NaCl + Br2
Cl2 + 2FeCl2 → 2FeCl3
3Cl2 + 6FeSO4 → 2Fe2(SO4)3 + 2FeCl3
Cl2 + 2KI → 2KCl + I2
Tác dụng với chất khử khác
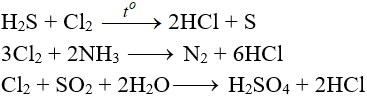
Phản ứng thế, phản ứng cộng, phản ứng phân huỷ với một số hợp chất hữu cơ
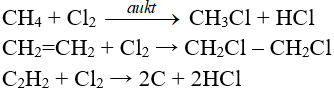 Tác dụng với dung dịch bazơ
Tác dụng với dung dịch bazơ
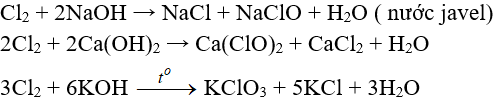
5. Cách thực hiện phản ứng
Mangan tác dụng với khí clo thu được muối
6. Bạn có biết
Mn là kim loại có tính khử nên dễ dàng tham gia phản ứng với các chất có tính oxi hóa mạnh như O2; Cl2 …
7. Bài tập liên quan
Ví dụ 1: Cho 19,2 g hỗn hợp gồm Al và Mn tác dụng vừa đủ với Cl2 thu được 51,15 g muối. Xác định khối lượng của Mn có trong hỗn hợp đầu :
A. 16,5g
B. 17,5g
C.18,5g
D.73,5g
Hướng dẫn giải:
Đáp án A
Ví dụ 2: Khi cho 5,5 g một kim loại R hoá trị II tác dụng với Cl2 thu được 12,6g muối. Tìm kim loại R?
A. Cu
B. Mn
C. Zn
D. Fe
Hướng dẫn giải:
Đáp án B
Ví dụ 3: Khi cho Mn tác dụng với khí clo thu được muối. Mn trong phản ứng đóng vai trò là chất gì?
A. Chất khử
B. Chất oxi hóa
C. Chất xúc tác
D. Chất môi trường
Hướng dẫn giải:
Đáp án A
Mn0 -2e → Mn2+
Xem thêm Một số phương trình phản ứng hóa học khác của Mangan (Mn), chi tiết khác:
CÔNG TY TNHH ĐẦU TƯ VÀ DỊCH VỤ GIÁO DỤC VIETJACK
- Người đại diện: Nguyễn Thanh Tuyền
- Số giấy chứng nhận đăng ký kinh doanh: 0108307822, ngày cấp: 04/06/2018, nơi cấp: Sở Kế hoạch và Đầu tư thành phố Hà Nội.
2021 © All Rights Reserved.